Lernen am Originalschauplatz
Salz. Ein Bodenschatz, welcher in Laufe der Geschichte von Altaussee eine tragende Rolle gespielt hat.
Bei deinem nächsten Schulausflug in die Salzwelten Altaussee erzählen wir dir ganz genau warum. Nimm an unserem speziellen Programm "Klassenzimmer unter Tage" teil, kombiniere theoretisches Wissen mit Praxis und das Gelernte bleibt noch besser in Erinnerung.
Geschichte zum Angreifen und zum Experimentieren. So macht Lernen Spaß!
Lehrer*innen aufgepasst:
Wir bieten dir hier sogar fertiges Exkursionsdesign kostenlos zum Download an! Einfach herunterladen und ausdrucken. Somit steht der thematischen Vorbereitung für den salziges Schulausflug nichts mehr im Wege.

Klassenzimmer unter Tage
Bei uns erhält jede Klasse ohne Aufpreis ein spezielles Salzwelten-Package. Dieses enthält:
- NEU: Kostenloses Exkursionsdesign zum Download (Ideal für die Vor- und Nachbereitung des Themas Salz im Unterricht)
- eine „Salzforscher-Tasche“
- verschiedene Salzprodukte
- detaillierte Informationen rund um das Thema Salz
- eine Anleitung für verschiedene Versuche
- einen kleinen Salzstreuer für jeden Schüler
- einen DIN A2-Jahresplaner als
Erinnerung an diese außergewöhnlichen Unterrichtsstunden unter Tage

Das Stollenquiz: 300 Euro für die Klassenkasse!
Wer gut während der Führung durch das Salzbergwerk aufpasst, hat die Möglichkeit 300 Euro für die Klassenkasse zu gewinnen!
Hol dir das "Stollenquiz" an der Salzwelten-Kassa ab und beantworte die Fragen so gut du kannst. Am Ende des Jahres verlosen wir das Preisgeld.
Packages für Schulklassen
Salzwelten und ...

Salzwelten Altaussee & Dachstein Höhlenwelten
- Eintritt und spezielle Schulführung "Klassenzimmer unter Tage" (Dauer: ca. 90 Minuten)
- Besuch der Rieseneishöhle (Dauer: ca. 2,5 Stunden)
- Berg- und Talfahrt mit der Dachstein Welterbe-Seilbahn, 1. Teilstrecke
Preis: 39,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei;
innerhalb von 5 Tagen einlösbar)

- Eintritt und spezielle Schulführung „Klassenzimmer unter Tage“ (Dauer: ca. 90 Minuten)
- 3-Seen-Tour einfach: Grundlsee – Toplitzsee – Kammersee
(Rückfahrt von Gössl mit dem eigenen Bus; Dauer ca. 2,5 Stunden)
Preis: 28,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)

- Eintritt und spezielle Schulführung "Klassenzimmer unter Tage" (Dauer: ca. 90 Minuten)
- Berg- und Talfahrt mit der Loser Panoramabahn
Preis: 22,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)

- Eintritt und spezielle Schulführung „Klassenzimmer unter Tage“ (Dauer: ca. 90 Minuten)
- Schulführung mit Kreativprogramm in der Sonderausstellung auf Schloss Trautenfels
Preis: 18,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)

Salzwelten Altaussee & Dachstein Höhlenwelten
- Eintritt und spezielle Schulführung "Klassenzimmer unter Tage" (Dauer: ca. 90 Minuten)
- Besuch der Rieseneishöhle (Dauer: ca. 2,5 Stunden)
- Berg- und Talfahrt mit der Dachstein Welterbe-Seilbahn, 1. Teilstrecke
Preis: 39,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei;
innerhalb von 5 Tagen einlösbar)

- Eintritt und spezielle Schulführung „Klassenzimmer unter Tage“ (Dauer: ca. 90 Minuten)
- 3-Seen-Tour einfach: Grundlsee – Toplitzsee – Kammersee
(Rückfahrt von Gössl mit dem eigenen Bus; Dauer ca. 2,5 Stunden)
Preis: 28,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)

- Eintritt und spezielle Schulführung "Klassenzimmer unter Tage" (Dauer: ca. 90 Minuten)
- Berg- und Talfahrt mit der Loser Panoramabahn
Preis: 22,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)

- Eintritt und spezielle Schulführung „Klassenzimmer unter Tage“ (Dauer: ca. 90 Minuten)
- Schulführung mit Kreativprogramm in der Sonderausstellung auf Schloss Trautenfels
Preis: 18,-- EUR pro Person
(Schulgruppen: jede 11. Person frei;
Jugendgruppen: jede 21. Person frei)
Unser Tipp:

MELDET EUCH ZUM SCHUL-NEWSLETTER AN!
Ihr wollt ab sofort immer up to date sein, was an unseren drei Salzwelten-Standorten so los ist? Welche speziellen Aktionen und Gewinnspiele es für Schulklassen gibt? Dann meldet euch doch gleich ganz easy & unkompliziert zu unserem neuen Schul-Newsletter an! Außerdem servieren wir euch mit dem Newsletter zusätzliches interessantes Salz-Wissen, das ihr im Unterricht verwenden könnt.
Gleich hier anmelden!Lehrer*Innen aufgepasst: Exkursionsdesigns
Hier findest du neben spannendem Salzwissen auch Versuchsanleitungen sowie verschiedenste Exkursionsdesigns zum Download. Damit kannst du deinen Schüler*Innen praxisnah alle wichtigen Details zum lebenswichtigen Mineral Salz näherbringen.
Salziges Wissen
Salz zählt zu den ursprünglichsten und wichtigsten Naturprodukten und ist für den Menschen unverzichtbar. Doch Salz ist nicht gleich Salz:Die verschiedenen Salzarten unterscheiden sich hinsichtlich Gewinnungsmethode und Ursprung.
Steinsalz: Im Salzbergwerk mit Tradition gewonnen
Steinsalz liegt im Gestein eingebettet und wird bergmännisch gewonnen. Die Salzbrocken werden dabei mit Werkzeugen aus dem Berg herausgebrochen und im Gegensatz zur Siedesalzgewinnung trocken abgebaut. Nachdem das Steinsalz aus dem Berg gebrochen wurde, wird es vorverlesen, zerkleinert und vermahlen. Nur hochreine Salzadern sind für dieses Trockenabbauverfahren geeignet.
Zu den Besonderheiten des Steinsalzes aus dem Salzkammergut zählen die Naturbelassenheit, die milde Geschmacksnote und die feine hell-beige Färbung. Die Farbe ergibt sich unter anderem durch den Eisengehalt und der einzigartigen Mineralstoffzusammensetzung. Wichtige Mineralstoffe und Spurenelemente wie Calcium, Magnesium und Eisenoxid machen es zu einer weltweiten Besonderheit.
Weitere bekannte Steinsalze sind unter anderem
- das rosafarbene Himalayasalz aus dem Salzgebirge in Pakistan
- das Kalaharisalz aus der Kalahariwüste oder
- das persische Blausalz aus dem Iran.
Die unterschiedlichen Farben werden durch unterschiedlich eingelagerte Mineralien erzeugt. Im Gegensatz zu unserem heimischen Steinsalz müssen diese nach Österreich importiert werden.
Steinsalz-Tipp: Das Steinsalz eignet sich aufgrund der Naturbelassenheit und dem milden Geschmack hervorragend für die bewusste Küche.
Von der Sole zum Siedesalz
Unser BAD ISCHLER Siedesalz findet seinen Ursprung im Urmeer und hat sich vor 250 Millionen Jahren in unseren Alpen abgelagert. Salz ist ein Mineral und besteht aus Natriumionen und Chloridionen. Seine chemische Bezeichnung lautet Natriumchlorid (Kochsalz, kurz NaCl).
Bei der Gewinnung von Siedesalz wird salzhaltiges Wasser, die sogenannte Sole, aus dem Berg gewonnen und anschließend in der Saline verdampft. Durch senkrechte Bohrungen wird zuerst Wasser in die Kaverne, ein unterirdischer Hohlraum, eingeleitet.
Das Wasser löst Salz aus dem Gestein. Man spricht hierbei vom Nassabbau von Salz. Diese Sole wird gereinigt und verdampft. Je weißer das Salz, desto reiner ist es.
Mit einem Natriumchlorid-Gehalt von über 99,6% zählt unser BAD ISCHLER Siedesalz zu den reinsten und hochwertigsten Kristallsalzen – gewonnen aus den österreichischen Alpen.
Siedesalz eignet sich nicht nur als Speisesalz, es ist auch in anderen Bereichen vielseitig einsetzbar:
- Als Pharmasalz für medizinische Zwecke
- In Form von Salztabletten zur Aufbereitung von Trinkwasser und zur Desinfektion von Schwimmbadwasser
- Als Industrie- und Viehsalz
Siedesalz-Tipp: Feines Siedesalz eignet sich ideal zum Fermentieren von Lebensmitteln.
Meersalz: Durch Sonne und Wind gereift
Meersalz entsteht durch die Verdunstung von Meerwasser in natürlichen Lagunen oder künstlichen Becken. Durch Sonne und Wind verdunstet das Wasser in den flachen Wasserbecken und die Salzkonzentration steigt an. Das Meerwasser wird bei immer weiter steigendem Salzgehalt in ein Erntebecken geleitet. Dort wird das Meersalz schließlich kristallisiert und aus dem Wasser geschöpft.
Meerwasser enthält rund 3,5 Prozent an gelösten Salzen. Das ist lediglich ein Durchschnittswert, denn der Salzgehalt unterscheidet sich von Gewässer zu Gewässer. In kühleren Meeren oder Meeresbecken mit Süßwasserzufuhr ist der Salzgehalt eher niedrig. Der Salzgehalt von Gewässern in Gebieten mit starker Verdunstung ist hingegen höher. Das Tote Meer weist beispielsweise einen Salzgehalt von circa 28 Prozent auf.
Typisch für das Meersalz ist die natürliche, grobe Kornstruktur. Im Meersalz sind geringe Mengen von Kalium, Magnesium und dem Spurenelement Mangan enthalten.
Meersalz-Tipp: Das grobkörnige Meersalz eignet sich gut zum Einreiben von Geflügel und Fleisch.
Unser Salz in Österreich bildete sich vor rund 250 Millionen Jahren. Doch wie gelangte das weiße Gold überhaupt in unsere Alpen?
Das kann anhand der „Barren-Theorie“ des schwedischen Geologen Carl Ochsenius von 1877 erklärt werden:

Das heiße Klima am Ende des Erdaltertums führte zu einem stärkeren Verdampfen des Wassers im Randmeer als vom Ozean nachfloss. Der Verdunstungsprozess dauerte Millionen von Jahre und führte zu typischen Ablagerungen der im Meerwasser gelösten Stoffe: Karbonate, Sulfate und Salze. Der vollständige Verdunstungsprozess dauerte so lange an, bis das gesamte Meerwasser gänzlich verdampft war.

Als vor etwa 100 Millionen Jahren die Alpen entstanden, wurde das Salz zusammen mit seinen Deckschichten von den Erdplatten überschoben. Mit der Hebung der Alpen wurden die Meeresablagerungen gekippt und zerbrochen. Die sehr weichen und formbaren Salzablagerungen wurden schließlich dort abgelagert, wo wir sie heute abbauen. Durch das Gewicht der Kalkgebirge werden die weichen, plastischen Salzstöcke nach oben gedrückt, dicht ummantelt von einer schützenden Tonschicht. Ein Vorgang der bis heute andauert.
„Auf Gold kann man verzichten, nicht aber auf Salz.“
Warum ist das so und welche Mengen Salz werden empfohlen?
Unser täglich Salz bringt uns Schmalz
Der Körper eines Erwachsenen enthält von Natur aus je nach Gewicht und Größe etwa 150 bis 300 g Salz. Natriumchlorid (Kochsalz, kurz NaCl) ist ein lebenswichtiger Mineralstoff für unseren Körper und für entscheidende Funktionen verantwortlich. Es reguliert den Blutdruck sowie auch den Flüssigkeitshaushalt. Zu wenig Salz kann somit wichtige Körperfunktionen beeinträchtigen.
Die Osmose, Grundlage für den Zellstoffwechsel, wird ausschließlich durch die Salzkonzentration in den Zellen gesteuert. Jede kleinste Aktivität unseres Körpers ist somit nur durch das Vorhandensein von Salz möglich.
Salz richtig dosiert
Doch wieviel Salz braucht der Körper? Die Weltgesundheitsorganisation WHO empfiehlt Erwachsenen eine maximale Salzaufnahme von ca. 5 Gramm pro Tag, um alle wichtigen Funktionen im Körper unterstützen zu können. Diese Menge entspricht in etwa einem Teelöffel Salz. Kinder benötigen weniger Gramm, entsprechend ihrem geringeren Energiebedarf.
Bei einer ausgewogenen Ernährung werden etwa drei Viertel des täglichen Salzbedarfs mit Nahrungsmitteln aufgenommen. Ein Viertel wird durch Speisesalz abgedeckt, das zum Kochen und Würzen verwendet wird. Das deutsche Bundesministerium für Risikobewertung empfiehlt, dass ein Erwachsener die Mindestmenge von 1,4 Gramm pro Tag nicht unterschreiten sollte, um den Salzverlust auszugleichen.
Menschen mit erhöhtem Energiebedarf, zum Beispiel Sportler, sollten auf eine ausreichende Salzzufuhr achten. Es gilt also die richtige Dosierung für den eigenen Körper zu finden.
Salzige Versuche
Versuch: Wasser löst Salz
Du benötigst
- Eine flache Glasschale
- Salz
- Gries
- Eine Lupe oder ein Mikroskop
Versuch
- Gib Wasser und einige Salzkristalle in die flache Glasschale
- Beobachte sie mit dem Vergrößerungsglas bzw. mit dem Mikroskop. Die Salzkristalle werden kleiner und kleiner, bis sie schlussendlich ganz verschwinden.
- Mache jetzt den gleichen Versuch mit Wasser und Gries. Was beobachtest du?
Versuch: Physikalische Trennmethoden
Du benötigst
- Wasserglas
- je 1 Löffel Salz und Gries
- Kaffeefilter
- Kochtopf
Versuch
- Gib in das Wasserglas sowohl Salz als auch Gries und rühre gut um, bis sich das Salz aufgelöst hat.
- Wenn du nun diese Mischung aus Salz, Wasser und Gries wieder in seine einzelnen Bestandteile trennen möchtest, musst du unterschiedliche Methoden anwenden.
- Den Gries kannst du herausfiltern, indem du den gesamten Inhalt des Glases durch einen Kaffeefilter gießt: der Gries bleibt sichtbar im Filter zurück. Koste nun das durch den Filter geflossene Wasser. Wurde auch das Salz herausgefiltert?
- Um das Salz aus dem Wasser herauszubekommen, musst du eine andere physikalische Trennmethode anwenden: du schüttest die Salzlösung in einen Kochtopf und bringst sie am E-Herd zum Sieden, und zwar so lange, bis das Wasser verdampft ist. Im Topf bleibt eine weiße Kruste zurück. Überprüfe nun den Geschmack des Rückstandes!
Versuch: 3 + 1 = 3 ??
Du benötigst
- Gurkenglas
- Salz
- Gries
Versuch
- Fülle das Gurkenglas zu etwa dreiviertel (ca. 0,5 Liter) mit Wasser und markiere den Wasserstand.
- Gib nun das Salz dazu, verrühre gut, bis sich das Salz aufgelöst hat. Überprüfe den Wasserstand.
- Zum Vergleich kannst du dasselbe mit der gleichen Menge Wasser und der gleichen Menge Gries versuchen. Was stellst du fest?
Erklärung
Ein „Salzkorn" besteht aus vielen winzig kleinen Teilchen, die man nicht sehen kann. Kommt ein Salzkörnchen mit Wasser in Kontakt, so bröckeln die kleinen Salzteilchen vom größeren Salzkorn ab.
Man muss sich Wasser so vorstellen, dass zwischen den einzelnen Wasserteilchen „Hohlräume" oder „Lücken" vorkommen. In genau diese Hohlräume „passen" die aufgelösten Salzteilchen. Sie verschwinden sozusagen in den Lücken und deshalb steigt der Wasserspiegel nicht!
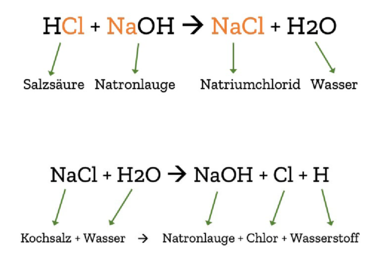
Wenn wir von Salz sprechen, so meinen wir meist Kochsalz. Allerdings gibt es in der Chemie eine Menge von Salzen. Salze entstehen, wenn man eine Säure mit einer Lauge vermischt.
Beim Kochsalz (chemisch: Natriumchlorid – NaCl) handelt es sich dabei um Salzsäure (chemische Formel: HCl) und Natronlauge (NaOH). Dabei entsteht Kochsalz und Wasser. Diese Verbindung aus Natrium und Chlor lässt sich auch wieder trennen.
Versuch: Zerlegung von Kochsalz in Natrium und Chlor
Du benötigst
- Gurkenglas
- 2 Drähte
- 3 Esslöffel Salz
- 4,5 Volt Batterie
- Wasser
Versuch
- Fülle das Glas mit Wasser, gib 3 Esslöffel Salz dazu und rühre so lange um, bis sich das Salz aufgelöst hat.
- Jetzt wickelst du je einen Draht um die beiden Pole der Batterie, die beiden anderen Enden hängst du in die Salzlösung. (Achtung: die beiden Drähte dürfen einander nicht berühren!)
- Jetzt beginnt es an den beiden Enden unterschiedlich stark zu blubbern. Der elektrische Strom trennt jetzt das Kochsalz in seine beiden Bestandteile Natrium und Chlor.
- An dem Draht, der mit dem Minuspol (der längere) verbunden ist, verbindet sich Natrium mit Wasser zu Natronlauge.
- Am Pluspol (der kürzere Pol der Batterie) steigen gelb-grüne Bläschen auf, Chlor, welches sich teilweise gleich wieder mit dem Kupfer zu Kupferchlorid verbindet. Wenn du vorsichtig in das Glas riechst, kannst du den typischen Chlorgeruch erkennen.
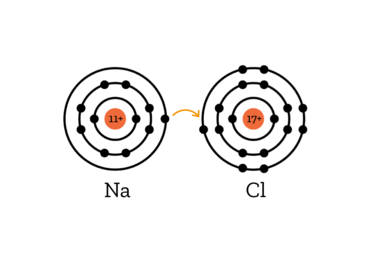
Erklärung
Wenn Salz in Wasser gelöst wird, wird die Verbindung von Natrium und Chlor gelöst. Dabei gibt das Natrium sein einziges Elektron der äußersten Schale an das Chlor ab, das nun 8 Elektronen in der äußersten Schale hat, was jedes Atom gerne haben möchte (die Chemiker nennen die den Edelgaszustand).
Das Natrium hat jetzt ein Elektron zu wenig und ist deshalb positiv geladen, wir sprechen vom Na+ -Ion.
Das Chlor hingegen hat nun ein Elektron mehr und ist jetzt negativ geladen, wir sprechen vom Cl- -Ion. (Ionen sind elektrisch geladenen Teilchen).
Wenn du nun eine Stromquelle (zwei Elektroden in die Lösung hängst), wandern die Cl - - Ionen zum Pluspol und geben dort ihr Elektron an den Pol ab. Somit sind sie elektrisch neutral und entweichen an diesem Pol als Chlorgas.
Die Na+ - Ionen wandern zu Minuspol, erhalten dort ein Elektron und es entsteht metallisches Natrium. Das reagiert aber sofort mit dem Wasser zu Natronlauge. Es entweicht Wasserstoff.
Bevor die Konservendose und der Tiefkühlschrank erfunden waren, wurde unter anderem Salz zum Haltbarmachen von Lebensmitteln verwendet.
Salz wird traditionell zur Konservierung von Fleisch (Pökeln, Suren), Fisch (etwa Salzhering), Gemüse (Sauerkraut) usw. verwendet. Bereits die Ägypter kannten diesen Trick und haben so ihre Speisen haltbar gemacht, auf Schiffsreisen wurde Pöckelfleisch mitgenommen.
Versuch: Essiggurken selbst herstellen
Du benötigst
- 1/2 kg kliene Gurken
- 1/4 Liter Essig
- 1/4 Liter Wasser
- 1 Esslöffel Salz
Versuch
- Die Gurken in eine Schüssel legen, mit kaltem Wasser bedecken und über Nacht stehen lassen. Dann abspülen und gut abtrocknen.
- Gurken (sowie Estragon, Dill sowie und Weinblätter zusammen mit den Pfefferkörnern) lagenweise in ein sauberes Gefäß schichten.
- Das Wasser mit dem Essig und dem Salz verrühren und über die Gurken gießen, so dass sie davon völlig bedeckt sind.
- Einen flachen Teller auf das Gefäß setzen und mit einem Stein beschweren.
- Die Gurken an einem kühlen Platz mindestens 4 Wochen stehen lassen, gelegentlich kontrollieren. Bildet sich nach einiger Zeit an der Oberfläche eine weißliche Hefeschicht, die Gurken abspülen und die Flüssigkeit erneuern.
Tipp!
Um Hefe- oder Schimmelbildung zu vermeiden, kann man die Gurkenlake zusätzlich mit etwas neutralem Speiseöl abdecken. Das Speiseöl lässt sich später ganz einfach mit einem Esslöffel wieder von der Oberfläche abnehmen.
Schon vor etwa 1500 Jahren kannten die Menschen im Fernen Osten die Möglichkeit, Speisen und Getränke zu kühlen. Dazu wird Eis zerstoßen und mit Salz vermengt. Die so entstandene "Kältemischung" kann unter idealen Bedingungen bis -21° abkühlen!
Diese Methode wurde erst Jahrhunderte später von Seefahrern nach Europa gebracht. Dazu wurden im Winter aus der Eisdecke von Seen und Flüssen Eisquader geschnitten, die dann in tiefen Erdkellern mit Stroh bedeckt gelagert wurden. Damit wurden dann im Sommer Getränke gekühlt. Wenn man besonders tiefe Temperaturen benötigte, zerstieß man das Eis und mischte es mit Salz, um die erwähnte Kältemischung zu erzeugen.
Versuch: Kältemischung
Du benötigst
- ca. 1/2 kg Eis oder Schnee
- 150 g Salz
- Gurkenglas
- Kochlöffel
- Hammer
- Geschirrtuch
Versuch
- Packe die Eiswürfel in das Geschirrtuch und lege es auf die schlagfeste Unterlage. Zertrümmere nun die Eiswürfel mit dem Hammer möglichst klein (Aufpassen, dass du nicht deine Finger erwischst!)
- Fülle nun 2-3 cm davon in das Gurkenglas, darüber streust nun eine etwa 1 cm dicke Schicht Salz, darüber wieder Eis usw.
- Rühre jeweils mit einem Kochlöffel um.
- Stecke nun bevor die Masse zu hart wird, das Thermometer in das Gemisch und verfolge, wie die Temperatur absinkt.
Erklärung
Wenn man Salz und Wasser vermischt, so möchte sich das Salz immer im Wasser lösen. Bei diesem Versuch muss aber erst das Eis geschmolzen werden, bevor sich das Salz im Wasser lösen kann.
Das Eis beginnt an der Oberfläche zu schmelzen, und sofort löst sich das Salz mit dem Wasser. Diese Reaktion benötigt aber auch Wärme, um überhaupt ablaufen zu können. Diese Wärme wird der Umgebung entzogen, welche dadurch immer weiter abkühlt. Dadurch entstehen Temperaturen bis -21° C!
Diese Technik war bereits den Römern bekannt. Die benutzten damals Salze, die sich an den Wänden der Pferdeställe gebildet hatten. Dabei handelt es sich nicht um Kochsalz, sondern um Salpeter, welches hauptsächlich aus Ammoniumnitrat besteht. Ammoniumnitrat entsteht, wenn Gülle von Bakterien zersetzt wird. Auch die Soldaten Napoleons nutzten diese Technik, die damals aber mehr ein Nebenprodukt der Herstellung von Schießpulver war. Das Schießpulver für die damaligen Gewehre wurde nämlich auch aus Salpeter, Holzkohle und Schwefel hergestellt.
Im Meer liegen und dabei ein Buch lesen - diese Bilder sieht man oft, wenn Fotos vom Toten Meer gezeigt werden. Nur dort kannst du dich fast wie auf einer Luftmatratze auf das Wasser legen. Das funktioniert, weil der Salzgehalt des Wassers sehr hoch ist.
Im Mittelmeer ist der Salzgehalt des Wassers bei ca. 3%. Im Toten Meer hingegen liegt er bei sagenhaften 30%! Nur ganz wenige Lebewesen können unter diesen Bedingungen überleben. Daher kommt auch der Name "Totes Meer". Ohne Schwimmbewegungen geht der Mensch im Süßwasser unter. Auch ein frisches Ei sinkt im Süßwasser zu Boden.
Versuch: Das schwebende Ei
Du benötigst
- Gurkenglas
- Esslöffel
- Salz
- 1 frisches Ei
Versuch
- Lege das Ei vorsichtig mit Hilfe des Löffels auf den Boden des Gurkenglases.
- Gib nun einen Esslöffel Salz ins Wasser und rühre vorsichtig um, damit das Ei nicht bricht. Was ist passiert?
- Gib mehr Salz zum Wasser bis das Ei aufschwimmt. Im Salzwasser ist der Auftrieb größer als im Süßwasser.
- Was kannst du tun, damit das Ei wieder zu Boden sinkt?
Erklärung
Grund für dieses Phänomen ist der physikalische Auftrieb: jeder Körper wird im Wasser leichter, und zwar genau um so viel, wie das verdrängte Wasser wiegt.
Ein 3 dm³ großer Stein wiegt in der Luft etwa 7,5 kg. Im Wasser wiegt er um 3 kg weniger, da er 3 dm³ Wasser (= 3 kg) verdrängt. Also wiegt er nur mehr 4,5 kg.
Wenn:
- das Gewicht größer ist als der Auftrieb (z.B. Eisen - 7,8 kg/dm³), dann geht der Körper unter
- das Gewicht kleiner ist als der Auftrieb (z.B. Holz - 0,5 kg/dm³), dann schwimmt der Körper
- das Gewicht gleich ist dem Auftrieb (z.B. Fisch), dann "schwebt" der Körper
Das Ei hat eine Dichte (=Gewicht von 1 cm³) von etwa 1,1 g/cm³. Süßwasser hat eine Dichte von 1 g/cm³ --> das Ei geht unter. Salzwasser aus dem Toten Meer hat eine Dichte von ca. 1,3 g/cm³ --> das Ei steigt nach oben.
Versuch
- Erhitze das Wasser in einem Wasser kocher oder in einem Topf.
- Gib ca. 4 Kaffeelöffel Salz in ein hitzefestes Glas und gieße ca. 150 ml heißes Wasser darauf. Ruhre um, bis sich das Salz vollständig aufeglöst hat.
- Wenn sich das Salz aufgelöst hat, wiederhole den Vorgang, bis sich das Salz nicht mehr ihm Wasser löst, die Flüssigkeit also „gesättigt“ ist. Sobald das Wasser „gesättigt“ ist, nimmt es kein Salz mehr auf. Das Salz setzt sich am Glasboden ab.
- Trenne nun das Wasser vom nicht mehr lösbaren Salz. Verwende dafür einen Kaffeefilter oder eine Küchenrolle. Fülle das Salzwasser in ein anderes Glas um.
- Wickle den Naturfaden um einen Bleistift und lege den Bleistift über das Glas. Der Faden muss mit dem Salzwasser in Kontakt sein.
- Stelle das Glas an einen warmen Ort. Du kannst es z.B. auf den Heizkörper stellen. Nun musst du geduldig sein und einige Tage abwarten.
Tipp! Je länger du wartest, desto größer werden die Kristalle!
Exkursionsdesign zum Download
Das Unterrichtsmaterial wurde sorgfältig in Zusammenarbeit mit dem Verein Land schafft Leben erstellt.
Hier findest du noch mehr Infos zum Thema Salz für deinen Unterricht.
Das Unterrichtsmaterial wurde sorgfältig in Zusammenarbeit mit dem Verein Land schafft Leben erstellt.
Hier findest du noch mehr Infos zum Thema Salz für deinen Unterricht.
Das Unterrichtsmaterial wurde sorgfältig in Zusammenarbeit mit dem Verein Land schafft Leben erstellt.
Hier findest du noch mehr Infos zum Thema Salz für deinen Unterricht.
Wissenswertes vor deinem Besuch
Die Themen des „Klassenzimmer unter Tage“ sind perfekt geeignet für Kinder zwischen 6 und 15 Jahren.
Die Führung "Klassenzimmer unter Tage“ dauert ca. 90 Minuten.
Um dich und die SchülerInnen optimal betreuen zu können, beschränken wir die Gruppengröße auf maximal 80 Personen. Wenn die Gruppe aufgeteilt wird, folgt die nächste rund 15 bis 30 Minuten später.
Im Altausseer Salzbergwerk herrscht das ganze Jahr über eine konstante Temperatur von rund 7 Grad Celsius. Unabhängig von Wetter und Jahreszeit ist es im Inneren des Berges also immer kühl. Bitte stelle deshalb sicher, dass die SchülerInnen warme Kleidung und festes Schuhwerk tragen. So steht spannenden Stunden im Salzberg nichts mehr im Wege!
Die Führungen finden in Deutsch oder Englisch statt. Weitere Sprachen sind über den " Salzwelten Destination Guide" gratis im App Store oder auf Google Play für das eigene Smartphone downloadbar.
Kostenlose Busparkplätze befinden sich in unmittelbarer Nähe zum Eingang des Salzbergwerks.

Jetzt reservieren
Reserviere gleich jetzt für deine Klasse unter der E-Mailadresse info@salzwelten.at oder telefonisch unter +43 61 32 200 2400 vor.
Kontakt

















